
多层级的质量管理
质量控制
PM监查
质量部
核查
项目组
互查
部门质控
专业全面的“标准操作流程”(SOP)
| SOP编号 | SOP名称 |
| SOP-MD-OP-001 | 医疗器械临床试验流程 |
| SOP-MD-OP-002 | 项目组内部沟通 |
| SOP-MD-OP-003 | 公司内部沟通 |
| SOP-MD-OP-004 | 公司外部沟通 |
| SOP-MD-OP-005 | 项目团队的建立 |
| SOP-MD-OP-006 | 项目组成员培训 |
| SOP-MD-OP-007 | 中心筛选及确认 |
| SOP-MD-OP-008 | 项目日常管理 |
| SOP-MD-OP-009 | 试验文档管理 |
| SOP-MD-OP-010 | 临床试验物资管理 |
| SOP-MD-OP-011 | 试验方案的起草、审核 |
| SOP-MD-OP-012 | ICF、CRF等资料起草、审核 |
| SOP-MD-OP-013 | 研究者会议 |
| SOP-MD-OP-014 | 独立伦理委员会的审批 |
| SOP-MD-OP-015 | 中心协议签署 |
| SOP-MD-OP-016 | 试验用医疗器械管理 |
| SOP-MD-OP-017 | 研究中心启动 |
| SOP-MD-OP-018 | 临床常规监查 |
| SOP-MD-OP-019 | 知情同意书监查 |
| SOP-MD-OP-020 | 原始数据溯源 |
| SOP-MD-OP-021 | 协同监查 |
| SOP-MD-OP-022 | 严重不良事件的处理及报告 |
| SOP-MD-OP-023 | 不良质量和欺诈行为的处理 |
| SOP-MD-OP-024 | CEC安全管理 |
| SOP-MD-OP-025 | 方案偏离的处理及报告 |
| SOP-MD-OP-026 | 质量控制 |
| ......... | ....... |
| SOP-MD-OP-037 | 临床试验数据交接 |
| SOP编号 | SOP名称 |
| SOP-MD-FM-001 | 项目文件夹一览表 |
| SOP-MD-FM-002 | 项目文档借阅表 |
| SOP-MD-FM-003 | 项目文件销毁清单表 |
| SOP-MD-FM-004 | 临床试验项目资料印刷 |
| SOP-MD-FM-005 | 中心联系名录 |
| SOP-MD-FM-006 | 员工培训签到表 |
| SOP-MD-FM-007 | 影像交接记录表(和CL) |
| SOP-MD-FM-008 | 研究者会议签到表 |
| SOP-MD-FM-009 | 临床试验物品交接表 |
| SOP-MD-FM-010 | 临床试验文件交接表 |
| SOP-MD-FM-011 | 医疗器械运送及接受记录表 |
| SOP-MD-FM-012 | 温、湿度记录表-内部(如适用) |
| SOP-MD-FM-013 | 温、湿度记录表-中心(如适用) |
| SOP-MD-FM-014 | 医疗器械分发记录表 |
| SOP-MD-FM-015 | 医医疗器械回收/退货记录表 |
| SOP-MD-FM-016 | 医疗器械入库清单 |
| SOP-MD-FM-017 | 器械接收(库存)和使用、回收及销毁记录 |
| SOP-MD-FM-018 | 试验文件销毁记录表 |
| SOP-MD-FM-019 | 医疗器械退货记录表 |
| SOP-MD-FM-020 | 受试者筛选/入组登记表 |
| SOP-MD-FM-021 | 受试者鉴认代码表 |
| SOP-MD-FM-022 | 完成试验受试者编码目录 |
| SOP-MD-FM-023 | 严重不良事件报告样表 |
| SOP-MD-FM-024 | 器械缺陷报告样表 |
| SOP-MD-FM-025 | 重大医学事件报告样表 |
| SOP-MD-FM-026 | 方案偏离表 |
| ...... | ........ |
| SOP-MD-034 | 受试者退出记录表 |
| SOP编号 | SOP名称 |
| SOP-MD-TP-001 | 项目进度汇报模板 |
| SOP-MD-TP-002 | 项目周报/月报 |
| SOP-MD-TP-003 | 项目简报 |
| SOP-MD-TP-004 | 保密协议 |
| SOP-MD-TP-005 | 项目运营管理计划 |
| SOP-MD-TP-006 | 项目监查计划 |
| SOP-MD-TP-007 | 项目预算表 |
| SOP-MD-TP-008 | 项目文件夹目录 |
| SOP-MD-TP-009 | 项目文件夹标签模板 |
| SOP-MD-TP-010 | 文件说明记录 |
| SOP-MD-TP-011 | 临床试验协议模板 |
| SOP-MD-TP-012 | 会议纪要 |
| SOP-MD-TP-013 | 研究者会议日程 |
| SOP-MD-TP-014 | 风险与问题列表 |
| SOP-MD-TP-015 | 会议邀请函 |
| SOP-MD-TP-016 | 会议任务分解模板 |
| SOP-MD-TP-017 | 研究者会议纪录 |
| SOP-MD-TP-018 | 递交信 |
| SOP-MD-TP-019 | 启动访视报告 |
| SOP-MD-TP-020 | 研究者简历 |
| SOP-MD-TP-021 | 临床前访视报告 |
| SOP-MD-TP-022 | 监查访视计划 |
| SOP-MD-TP-023 | 启动前确认清单 |
| SOP-MD-TP-024 | 访视确认函 |
| SOP-MD-TP-025 | 访视后总结信 |
| SOP-MD-TP-026 | EDC监查报告模板(如适用) |
| ........ | ...... |
| SOP-MD-TP-065 | ICF/CRF |
网络化的管理流程
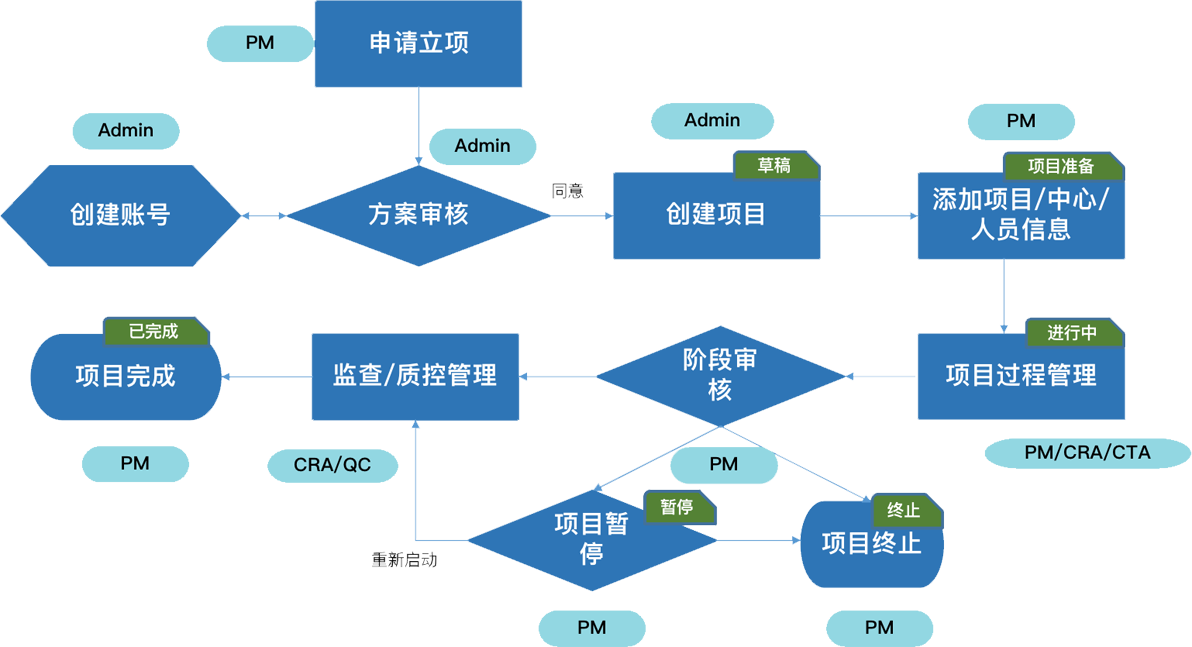
全面详尽的沟通机制
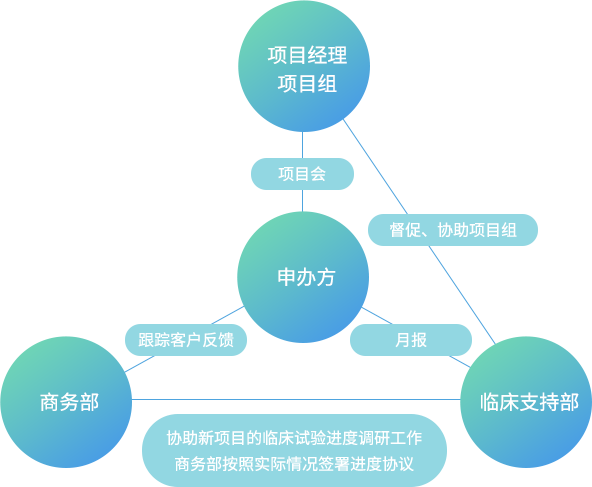
丰富的实操经验
注册方面优势